新型冠状病毒肆虐,药物是抗击新冠肺炎疫情的重要武器。疫情当前,对药物的临床需求十分紧迫。虽然科研人员争分夺秒地寻找药物应对此次疫情,但药物研发是一个周期长、成本高、成功率低的过程。
在公众生命受到严重威胁的当口,如何整合全球医药大数据资源,迅速为社会研发出安全、有效和可用的药品,是每一个新药研发企业的责任。
新药的研发有其客观规律和评审规范,需要周期较长。面对国际上新药研发投入逐年增高且失败率逐年增大的趋势,挖掘已有药物的抗病毒活性,能够在一定程度上加快研发速度、规避研发风险、降低研发成本,从而迅速满足临床用药需求。
开发、融合和借鉴国际上适应症挖掘的前沿技术,将有助于企业研发出符合我国国情的旧药新用。如果能通过医药大数据筛选和活性预测,找到廉价药物或中药的适应症拓展机会,进而产出具自主知识产权的适应症专利和新药批文,不仅可以迅速挽救生命和阻断疫情,更能从战略上为我国带来长远的社会和经济效益。
1. 新冠病毒肺炎最新药物研发情况
病毒肆虐,而新药的从头研发周期长、投入高、成功率低。对于我国这样一个人口众多而人均医药资源有限的国家来说,挑战巨大。
紧要关头,在目前还没有特效药的情况下,国内也在积极推进一批已上市药物、或者至少已经具备一定临床研究基础的药物,开展抗新冠病毒肺炎新适应症药物研发。
目前,我国科学家也在旧药新用领域积极展开对药物新适应症的探索(截至 2020 年 2 月,详情如下表)。
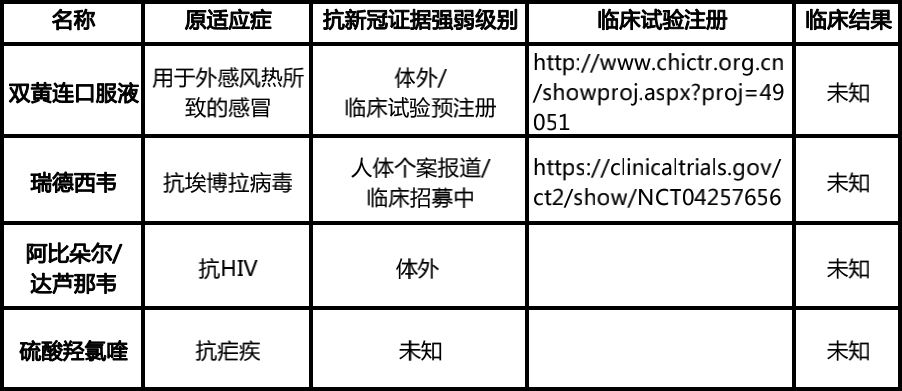
△ 表 1:新冠病毒肺炎最新药物研发一览表
如上海药物所的蒋华良院士连同武汉病毒所在体外实验率先初步证明,中药双黄连具有病毒抑制的效果;又如国家卫健委李兰娟院士近期初步测试出阿比朵尔和达芦那韦(抗 HIV)两款药物能体外有效抑制冠状病毒;就在本周,科技部宣布一种抗疟疾的旧药硫酸羟氯喹极可能对新冠肺炎有效,已被国家科技部、卫健委作为临床试验药物,如果属实,30 元不到一盒的价格,的确可以给病人带来希望。
2. 药物研发为何如此艰难?
针对新病毒去设计出对症的新药,从靶点发现、潜在药物空间、药物筛选再到临床试验、药品申报是一个极其漫长的过程。一个在实验阶段对病毒有效的药物,在进入人体后面临的状态又极为复杂,可能与人体内部系统之间发生更为复杂的变化,而不同人身体上生理差异性又将影响药效的发挥……可以说,新药研发不是一蹴而就的事情。
从已上市或已接近临床的现有药物中去筛选可能对有 2019-nCoV 有效的药,是许多科研团队当下正在抓紧做的事情。从科学严谨的角度来说,我们必须要指出,公众所期待的突然从天而降一款能完全对症该病毒的「神药」,是一件可能性微乎其微的事情。
此次的「新冠」疫情对于我国的生物医药行业来说也许是一个警钟,让我们看到中国抗病毒领域创新药研发能力和投入较国外仍有较大差距。
然而,全球有数十万个上市和在研药物,外加博大精深、种类繁多的中药,如果能通过医药大数据来挖掘旧药新用的机会,从已知老药中筛选候选新药,实现「大海捞针」,不仅可以加快挽救生命和阻断疫情的速度,更能从战略上为我国带来长远的社会和经济效益。
3. 旧药新用或可成为我国特色的新药研发之路之一?
药物重定位,也称为旧药新用,是指对已有的药物进行重新筛选、组合或改造从而发现其未知新用途的过程[1],长久以来都是一个不可或缺的药物开发方式。相比于从零开始的新药研发,药物重定位基于已有药物的重新开发能够节省大量前期研发投入(如药靶发现、化合物筛选、安全性测试等),可进一步扩大一个药物的适应症范围和销售市场。
同时,相对于传统的新药发现,药物重定位能够把药物的研发周期从 10-17 年缩短到最快几个月,因此越来越受到政府部门、制药企业、学术机构等各方面的关注。
比如,美国国立卫生院( NIH )近期发起大规模的药物重定位项目,鼓励各机构开放所拥有的候选化合物的部分知识产权,并加强多机构的交叉合作,发现旧化合物的潜在新疗效。 包括葛兰素史克、辉瑞、阿斯利康和罗氏等在内的各大制药公司纷纷为 NIH 项目贡献化合物。据咨询公司 BioVista 统计,世界前 20 大制药企业的利润已有至少 30% 来自于药物重定位。
尽管随着我国对生物医药领域的投入增多,国内研发的硬件条件得到了很大的提高,但相对于新药研发的巨额投入而言,仍然不得不认真思考如何利用有限的资源实现成果产出最大化和研发风险最小化这一关键问题。
药物重定位作为一种国际上被广泛采用的研发战略,具有更高的投入产出效率,值得我国产学研各界的关注和投入[2-3]。
4. 基于大数据的系统性药物重定位
传统的药物重定位主要通过临床观察和经验推测来偶然地发现药物引起的未知表型变化。一个经典的案例是西地那非(商品名:伟哥),它原本在临床试验中用于治疗心绞痛,然而通过仔细审视其副反应发现它还具有治愈勃起障碍的潜在功效[4]。再比如,醋酸艾塞那肽原本用于治疗二型糖尿病,在临床试验中却被发现具有减轻体重的「副」作用[5]。
然而上述发现均为「妙手偶得」,具有很大的偶然性和主观成分,不能被大范围推广并从根本上改善药物开发的效率。
现代药物研发需要创新性的、系统性的和可重复的药物重定位方法,将医药大数据在人工智能(AI)的平台上进行充分挖掘和利用是解决问题的钥匙之一。医药大数据包括基因组,转录组,蛋白组,代谢组以及临床表型大数据等。基于大数据的药物重定位在研发的内在逻辑上与传统的药物开发有异曲同工之处。
前者一般是基于同一致病靶蛋白或同一(或类似)疾病表型谱寻找新的化合物,而后者将这一逻辑进行拓展,扩大到基于同一(或类似)基因组表达谱、全基因组关联位点谱、化合物-蛋白互作组以及临床副作用情况等方面来链接旧药和新病之间的关系,更加系统和高效。
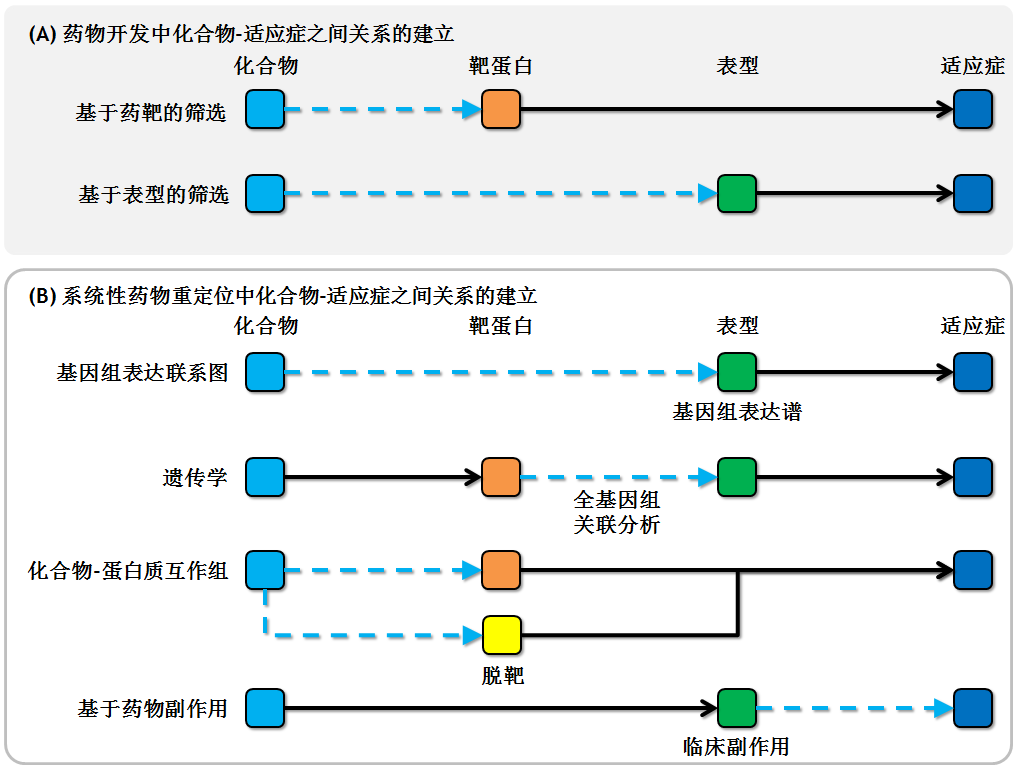
△ 图 1:药物开发(A)与基于大数据的系统性药物重定位(B)在联通化合物和适应症之间关系的策略
△ 药物两者在本质上具有很多共同的逻辑,都是通过各种手段打通药物、药靶、表型和疾病四个节点之间的路径 △ 药物图中实线表明已有的关系,而虚线代表有待建立的关系
全球范围内,目前通过大数据和 AI 开展旧药新用的公司也在国际资本市场中受到了关注。
美国公司 Recursion Pharmaceuticals 利用 AI 在数百种细胞模型上并行测试数千种化合物。2016 年,创立三年后,他们宣布与制药巨头赛诺菲合作,帮助后者确定一些研发管线的分子在几十种遗传疾病中可能的新用途。
此外,赛诺菲也与英国初创企业 Exscientia 签署了合作协议,计划使用后者的 AI 平台寻找代谢疾病治疗。
安斯泰来( Astellas )则比较关注重新利用现有化合物。2015 年 12 月,他们与初创公司 Biovista 宣布合作,主攻药物重定位的 AI 技术。一个月后,又和另一家初创公司 NuMedii 宣布合作,做类似的工作(该数据来源:站长之家)。
根据此指导思想,我们将详细介绍上图中最下方的两类成熟方法论——基于化合物-蛋白质互作组,以及基于药物副作用的人工智能和大数据方法,来对所有的已上市和在研药物进行适应症筛选,重点放在为国家重大紧急医疗需求(例如新型冠状状病毒抑制)、老年相关疾病、重症、罕见病等。旨在通过该方法论联通主流制药企业,拓展其拳头产品的适应症空间,帮助企业实现社会责任和经济效益的双赢。

△ 图 2. 人工智能新药研发平台赋能药厂、提升制药企业社会责任的示意图
4.1 基于化合物-蛋白质互作组寻找药物新靶点
在传统的基于靶蛋白的药物研发中,研究者会通过计算机模拟和实验方法,从海量的化合物库中筛选出与靶蛋白产生相互作用的先导化合物,再从这些化合物中筛选药物分子。而在基于化合物-蛋白质互作组的药物重定位研究中,作为起点的化合物就是经 FDA 审批的和制药公司正在研发中的药物分子。
在实际应用中,这些小分子药物除了和靶蛋白结合,还会和一系列其他人类蛋白发生相互作用[6],即存在「脱靶」效应(off-target)。「脱靶」效应一方面会引发药物不良反应[7],另一方面也创造了药物重定位的机会。
我国科研工作者为此开发出了「化合物-蛋白互作组」(Chemical-protein interactome,简称CPI)[8]的研究项目。CPI 尽可能地穷尽了全部的上市药物和全部的人类可药性蛋白,进而得到了记录各种靶药「对子」结合强度的数据矩阵。
对该矩阵进行变换和统计分析,可以系统校正特定「化合物-蛋白」对子的结合强度及其背景分布,从而有效地规避模拟中的常见偏差,提高信噪比[9-10]。该方法已经成功地阐明部分导致药物副反应的脱靶效应[11],其预测的药物与蛋白的非预期性结合也能被另一个独立研究组通过 X 射线晶体衍射所证实[12]。
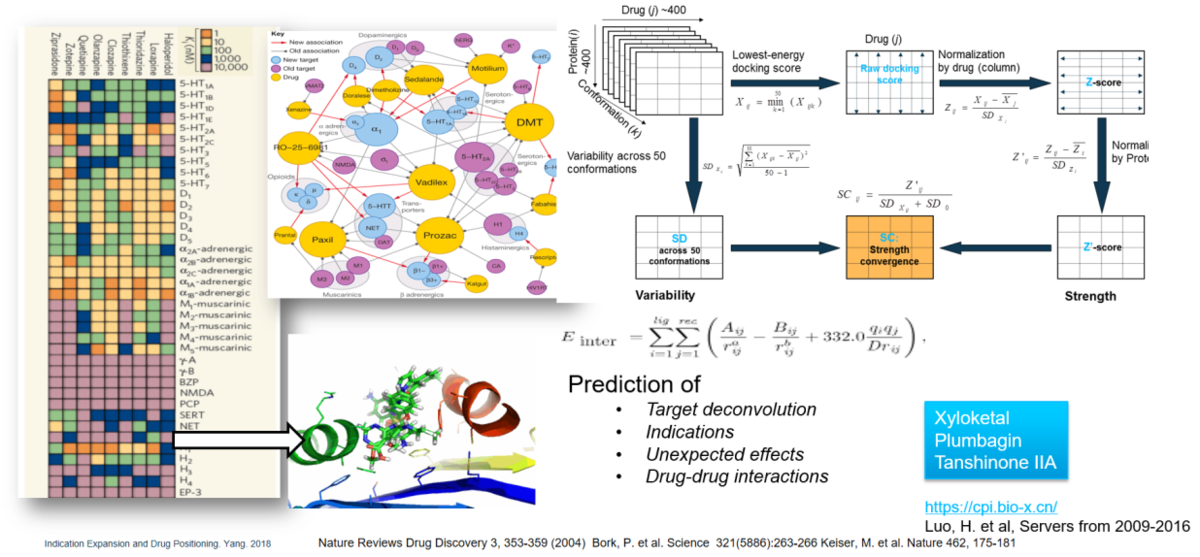
△ 图 3. 基于「化合物-蛋白互作组」进行药物重定位的原理
在 CPI 的基础上,用于药物重定位研究的在线服务器 DRAR-CPI 也已被开发出来(http://cpi.bio-x.cn/drar/)。用户在线提交一个感兴趣的「旧药」分子,后台程序便会自动在一个云计算平台上模拟计算出其与一系列人类蛋白的结合强度(图 4),形成一个「结合强度谱」;同时可以分析出具有相似「结合强度谱」的其他药物,列出它们已知的适应症。
具有相似结合强度谱的药物之间很可能具有相似的作用机理和适应症,因此这种分析可以为这个「旧药」间接匹配到新的候选适应症,高效率地辅助药物重定位的研究。
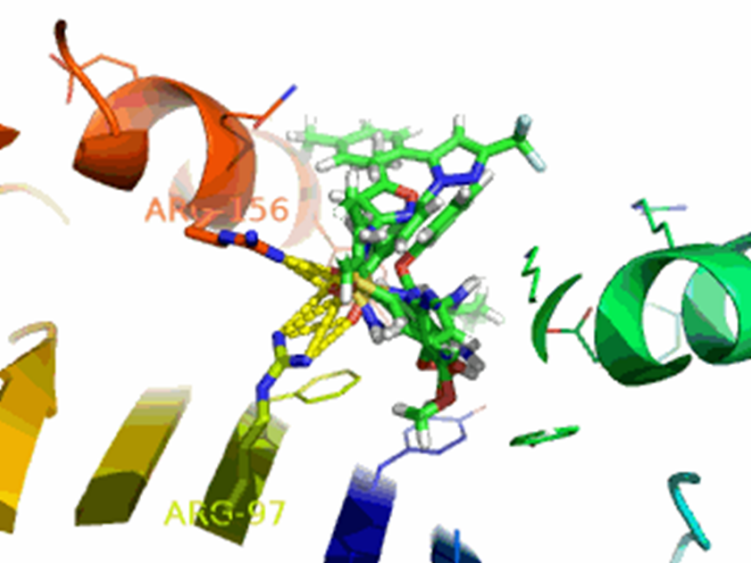
△ 图 4. 人工智新药研发平台率先发掘的药物 abacavir 和人类蛋白之间的互作关系
4.2 基于药物副作用的药物重定位
临床中所观测到的药物副作用可以作为药物重定位挖掘的另一个重要数据来源(side effect-based repositioning)。这些副作用信息通常被理解为药物安全性「风险」;但随着药物大数据和人工智能技术的发展,我们已经能从副作用信息中发现潜在的「旧药新用」线索,将「风险」转化成「机会」。
近期一项系统的药物重定位研究全面收集了与药物相关的副反应信息,并评估了用这些信息来预测药物新用途的精度[13]。该研究的基本假定是,药物的治疗效果和副反应都是药理学效应,两者密不可分,副反应可以作为「药物反应的生物标志物」来表征药物潜在的治疗用途(图 5)。
例如,治疗器官移植排异的药物在临床上常有的副作用是导致较高比率的巨细胞病毒感染。因为排异药物往往是免疫抑制剂,而免疫系统被抑制后,病毒感染的概率就增加了。数据显示,药物甲氨蝶呤具有增加病人巨细胞病毒感染几率的副作用,因此,我们推测该药物可能可以用于治疗器官移植排异。
事实上,确实已有研究在尝试使用该药作为移植排异的治疗,并且疗效显著[14]。由于副作用信息作为临床层面的直接证据,在研究层面强于细胞水平和动物模型水平的药理学证据,因此上述思路已被葛兰素史克采用来进行其药物重定位的研发[15]。
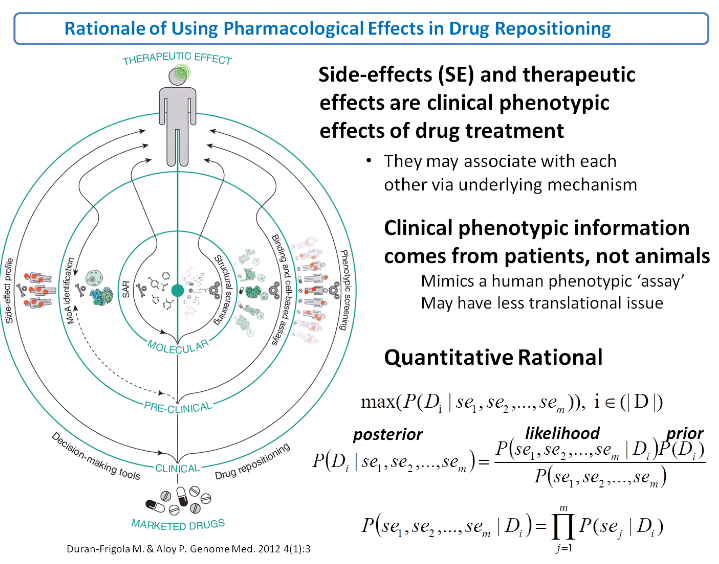
△ 图 5. 基于副作用的药物重定位原理
我国具有全世界最庞大的医药市场之一,国内外生产的大多数药物在我国都有规模可观的服药人群。而且随着医疗体系的不断升级和完善,越来越多的药物导致的副作用信息将被收集和记录在医药大数据库中。这些信息不仅有助于监控用药安全,还将有望成为促进我国新药研发的重要资源。
5. 在大数据和 AI 的时代背景下,旧药新用发现新机遇
事实证明,即便集中最优质的资源和大量的资本,基于传统流程的新药开发仍是一项高投入、长周期且高风险的研发工作。因此可以预见,系统性药物重定位及其相关的创新开发方法在未来的药物研发中将不仅仅是一项替代策略,而是会随着大数据和 AI 的不断介入而逐渐成为一种主流战略。
这一趋势的变化,对我国的药物研究和制药产业都将具有深远的影响。我国是一个人口众多而人均科研和医疗资源都非常有限的发展中国家,如何提高的药物的研发效率并降低失败率显得尤为重要。随着国内外生物技术和医药科学的长足发展,产学研各界已经积累了并且还在产生着大量的与疾病和药物相关高通量组学数据和以电子病历数据为代表的医药大数据。
如果能够加强医药大数据和 AI 的投入,建立具备处理医药大数据的云计算平台,并开发诸如 AIdPharma 一系列对高通量数据进行分析和解读的方法,就能够通过低成本和系统性的方式(而非基于偶然的实验或临床发现)发掘出数据的最大价值,并最终降低药物开发的成本和风险。
此外,我国还拥有一种独特的药物研究资源,即丰富且宝贵的中医药开发经验和数据积累。如果能够进一步完善中药组学数据的产生和挖掘技术,则有望利用其中蕴藏的巨大机会,使历史悠久的中医药更加历久弥新,带来更大的社会和经济效益。 疫情当前,当公众对新药研发的关注上升到前所未有的高度,我们希望通过人工智能和大数据来提升病人参与新药研发的积极性和话语权,利用药物重定位加速新药从临床前研究走向市场,在旧药新用的历史机遇中赋能更多传统制药企业。
本篇文章由企业社会价值研究院的专家团队出品,他们基于对医疗领域的学术研究及对商业的洞察,为我们带来了此次针对新型冠状病毒期间的药品研发、生物医药前沿技术的深度分析。
本文作者简介:
孙丽雅 上海交通大学生物医学博士后,企业社会价值研究院特约顾问
顾问团队:
杨仑 博士上海交通大学兼职教授,美国 FDA 访问学者,企业社会价值研究院特约顾问
田维维 慕尼黑大学药物学博士,清华大学化学学士,前拜耳医疗保健部门新产品开发副总监 ,企业社会研究院特约顾问
陆金华 美国 FDA 博士后 ,美国国防医科大学博士,曾任美国 FDA 生物制品审评和研究中心专家审评员,企业社会价值研究院特约顾问
谢清 博士 美国葛兰素史克(费城)研发中心总监 ,企业社会价值研究院 特约顾问
*参考文献:
[1]Chong CR, Sullivan DJ, Jr.: New uses for old drugs. Nature 2007, 448(7154):645-646.
[2]谢达菲, 李非, 伯晓晨, 王升启: 药物重定位的计算分析方法:研究综述. 生物化学与生物物理进展 2012.
[3]张永祥, 程肖蕊, 周文霞: 药物重定位——网络药理学的重要应用领域. 中国药理学与毒理学杂志 2012(6):779-786
[4]Ghofrani HA, Osterloh IH, Grimminger F: Sildenafil: from angina to erectile dysfunction to pulmonary hypertension and beyond. Nat Rev Drug Discov 2006, 5(8):689-702.
[5] Buse JB, Henry RR, Han J, Kim DD, Fineman MS, Baron AD, Exenatide-113 Clinical Study G: Effects of exenatide (exendin-4) on glycemic control over 30 weeks in sulfonylurea-treated patients with type 2 diabetes. Diabetes care 2004, 27(11):2628-2635.
[6]Li H, Gao Z, Kang L, Zhang H, Yang K, Yu K, Luo X, Zhu W, Chen K, Shen J et al: TarFisDock: a web server for identifying drug targets with docking approach. Nucleic acids research 2006, 34(Web Server issue):W219-224.
[7]Lounkine E, Keiser MJ, Whitebread S, Mikhailov D, Hamon J, Jenkins JL, Lavan P, Weber E, Doak AK, Cote S et al: Large-scale prediction and testing of drug activity on side-effect targets. Nature 2012, 486(7403):361-367.
[8]Yang L, Wang K, Chen J, Jegga AG, Luo H, Shi L, Wan C, Guo X, Qin S, He G et al: Exploring off-targets and off-systems for adverse drug reactions via chemical-protein interactome--clozapine-induced agranulocytosis as a case study. PLoS Comput Biol 2011, 7(3):e1002016.
[9]Yang L, Chen J, Shi L, Hudock MP, Wang K, He L: Identifying unexpected therapeutic targets via chemical-protein interactome. PLoS One 2010, 5(3):e9568.
[10]Yang L, Luo H, Chen J, Xing Q, He L: SePreSA: a server for the prediction of populations susceptible to serious adverse drug reactions implementing the methodology of a chemical-protein interactome. Nucleic acids research 2009, 37(Web Server issue):W406-412.
[11]Yang L, Chen J, He L: Harvesting candidate genes responsible for serious adverse drug reactions from a chemical-protein interactome. PLoS Comput Biol 2009, 5(7):e1000441.
[12]Ostrov DA, Grant BJ, Pompeu YA, Sidney J, Harndahl M, Southwood S, Oseroff C, Lu S, Jakoncic J, de Oliveira CA et al: Drug hypersensitivity caused by alteration of the MHC-presented self-peptide repertoire. Proceedings of the National Academy of Sciences of the United States of America 2012, 109(25):9959-9964.
[13]Yang L, Agarwal P: Systematic drug repositioning based on clinical side-effects. PLoS One 2011, 6(12):e28025.
[14]Cahill BC, O'Rourke MK, Strasburg KA, Savik K, Jessurun J, Bolman RM, 3rd, Hertz MI: Methotrexate for lung transplant recipients with steroid-resistant acute rejection. The Journal of heart and lung transplantation : the official publication of the International Society for Heart Transplantation 1996, 15(11):1130-1137.